중학교 2학년 과학 7단원 수권과 해수의 순환
해수의 특성
1. 해수의 온도
1) 표층 해수의 온도
표층의 해수 온도는 위도에 따라 달라 진다.
-> 위도에 따라 해수면에 도달하는 태양 에너지의 양이 차이가 나기 때문이다.

저위도 해역은 해수면에 도달하는 태양 에너지의 양이 많기 때문에 표층 해수의 수온이 높다.
고위도 해역은 해수면에 도달하는 태양 에너지의 양이 적기 때문에 표층 해수의 수온이 낮다.
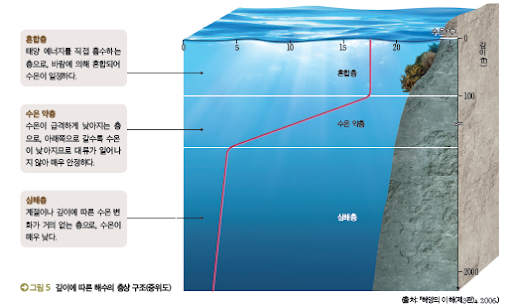
2) 깊이에 따른 해수의 온도
깊이에 따른 수온 분포를 기준으로 혼합층, 수온 약층, 심해층의 층상 구조를 이룬다.

(*수온 약층은 혼합층과 심해층 사이에서 열이나 물질이 교환되는 것을 차단한다)
2. 해수의 염분
1) 염류 : 해수에 녹아 있는 여러 가지 물질
1. 염류의 종류 : 짠맛이 나는 염화 나트륨, 쓴맛이 나는 염화 마그네슘, 황산 마그네슘, 황산 칼슘 등이 있다.
2. 염류의 비율: 염화 나트륨>>염화 마그네슘>황산 마그네슘>황산 칼슘
2. 바닷물 1000g에는평균적으로 약 35g의 염류가 녹아 있다

2) 염분 : 해수 1000g에 녹아 있는 염류의 양을 g 수로 나타낸 것이다
1. 단위 : pus또는 ‰ (퍼밀)을 사용한다
2. 전 세계 해수의 평균 염분은 약 35pus이고, 우리나라 주변 바다의 편균 염분은 약 33pus이다.
3) 염분에 영향을 주는 요인 : 증발량과 강수량의 차이, 육지에서 흘러드는 물의 양, 빙하가 녹거나 해수가 어는 정도 등이 영향을 준다.
염분이 낮은 해역 : 육지의 물이 흘러드는 해역, 빙하가 녹는 해역, 증발량보다 강수량이 많은 해역
염분이 높은 해역 : 해수가 어는 해역, 강수략보다 증발량이 많은 해역
4) 염분비 일정 법칙
1. 해수의 염분이 높고 낮음에 관계없이 해수에 녹아 있는 각 염류가 차지하는 비율은 일정하다는 것이다.
2. 해수에 들어 있는 염류의 비율


(* 염류의 비육 구하기
각 염류의 양(g)/전체 염류의 양(g) x 100 )